Công ty THT Việt Nam luôn áp dụng các tiêu chuẩn kỹ thuật cơ bản của Tổ chức y tế Thế giới (WHO) và các tổ chức khác của Mỹ với các phiên bản tài liệu được cập nhật mới nhất khi thực hiện thiết kế và lắp đặt các dự án phòng an toàn sinh học và phòng sạch (Bao gồm các dây chuyền sản xuất vắc xin, dược phẩm và bao bì dược phẩm, các phòng kiểm nghiệm dược phẩm, các kho bảo quản nguyên liệu và dược phẩm, các nhà máy sản xuất thiết bị và linh kiện điện tử, v.v...). Các tiêu chuẩn thiết kế cơ bản của chúng tôi gồm có:
Các tiêu chuẩn thiết kế cơ bản của Công ty THT Việt Nam:
a. Các tiêu chuẩn chính:
- Các tiêu chuẩn GMP (Thực hành tốt sản xuất thuốc), GLP (Thực hành tốt kiểm nghiệm thuốc), GSP (Thực hành tốt bảo quản thuốc) của Tổ chức Y tế Thế giới (WHO).
- Hướng dẫn về An toàn sinh học của WHO, phiên bản 3.
b. Các tiêu chuẩn liên quan :
- Tài liệu HVAC của Hiệp hội kỹ sư Mỹ về nhiệt lạnh và thông khí (ASHRAE).
- Hướng dẫn an toàn sinh học và vi sinh trong phòng thí nghiệm của NIH (Mỹ) - Phiên bản 4.
- Các tài liệu của Trung tâm Kiểm soát và Ngăn ngừa Dịch bệnh (CDC - Mỹ).
v.v …
I - TIÊU CHUẨN GMP-WHO:
1. Giới thiệu về GMP-WHO:
- GMP là những chữ viết tắt bằng tiếng Anh của “Good Manufacturing Practice" (Thực hành tốt sản xuất).
- Thực hành sản xuất tốt bao gồm những nguyên tắc chung, những quy định, hướng dẫn các nội dung cơ bản về điều kiện sản xuất; áp dụng cho các cơ sở sản xuất, gia công, đóng gói thực phẩm, dược phẩm, thiết bị y tế, mỹ phẩm …, nhằm đảm bảo sản phẩm đạt chất lượng và an toàn.
- GMP quan tâm đến các yếu tố quan trọng: con người, nguyên vật liệu, máy móc thiết bị, thao tác, môi trường ở tất cả các khu vực của quá trình sản xuất, kể cả vấn đề giải quyết khiếu nại của khách hàng và thu hồi sản phẩm sai lỗi.
- Những yêu cầu của GMP có tính mở rộng và tổng quát, cho phép mỗi nhà sản xuất có thể tự quyết định về số quy định, tiêu chuẩn, thủ tục, hướng dẫn công việc sao cho đáp ứng được các yêu cầu cần thiết, phù hợp với loại hình, lĩnh vực sản xuất và điều kiện cơ sở vật chất của doanh nghiệp. Chính vì vậy số các quy định, thủ tục của hệ thống GMP của mỗi doanh nghiệp sẽ khác nhau.
2. Phạm vi và đối tượng kiểm soát của tiêu chuẩn GMP:
- Nhân sự.
- Nhà xưởng.
- Thiết bị.
- Vệ sinh sản xuất, vệ sinh môi trường, vệ sinh cá nhân.
- Quá trình sản xuất: thao tác của công nhân, thực hiện các yêu cầu về nguyên vật liệu, về tiêu chuẩn sản phẩm, công thức pha chế, về điều kiện vật chất của sản xuất, đánh giá việc cung ứng của nhà cung cấp nguyên vật liệu
- Chất lượng sản phẩm: thử nghiệm mẫu
- Kiểm tra: nguyên liệu, bán thành phẩm, sản phẩm, thao tác của công nhân, đánh giá nhà cung ứng, vệ sinh
- Xử lý sản phẩm không phù hợp, giải quyết khiếu nại của khách hàng
- Tài liệu, hồ sơ thực hiện …
3. Hệ thống tài liệu của tiêu chuẩn GMP cho mỗi quy trình sản xuất bao gồm:
3.1. Các Quy phạm sản xuất theo tiêu chuẩn GMP: là quy định các thao tác, vận hành trong công nghệ và thiết bị, quy định thành phần nguyên vật liệu trong từng công đoạn sản xuất, quy định tiêu chuẩn của sản phẩm được xây dựng cho từng sản phẩm hoặc nhóm sản phẩm tương tự, của từng công đoạn hoặc một phần công đoạn sản xuất trong quy trình công nghệ chế biến thực phẩm
a. Nội dung Quy phạm sản xuất GMP có 4 phần:
- Mô tả rõ yêu cầu kỹ thuật hoặc quy trình chế biến tại công đoạn hoặc một phần công đoạn sản xuất đó.
- Nêu rõ lý do phải thực hiện các yêu cầu hoặc quy trình kỹ thuật đã nêu.
- Mô tả chính xác các thao tác, thủ tục phải tuân thủ tại công đoạn hoặc một phần công đoạn sản xuất nhằm đảm bảo đạt được yêu cầu chất lượng, đảm bảo an toàn vệ sinh cho sản phẩm, phù hợp về tiêu chuẩn kỹ thuật.
- Phân công cụ thể việc thực hiện và quy định giám sát việc thực hiện GMP.
b. Hình thức Quy phạm sản xuất GMP: được thể hiện dưới dạng văn bản, gồm hai phần:
- Các thông tin về hành chính (tên, địa chỉ công ty, tên sản phẩm hoặc nhóm sản phẩm, số và tên quy phạm, ngày và chữ ký phê duyệt của người có thẩm quyền).
- 4 nội dung chính nêu trên.
3.2. Các Quy phạm vệ sinh tiêu chuẩn SSOP (Sanitation Standard Operating Procedure): là các quy trình, thủ tục, hướng dẫn làm vệ sinh nguồn nước, nhà xưởng, thiết bị chế biến và những bề mặt tiếp xúc trực tiếp với sản phẩm, vệ sinh cá nhân … và các thủ tục kiểm soát vệ sinh tại nơi sản xuất. Quy phạm vệ sinh chuẩn được xây dựng và áp dụng để đạt được các yêu cầu về vệ sinh chung của GMP.
a. Nội dung của Quy phạm vệ sinh chuẩn gồm 4 phần:
- Yêu cầu (hoặc mục tiêu) của doanh nghiệp và các quy định của cơ quan có thẩm quyền.
- Điều kiện hiện có: Mô tả điều kiện cơ sở vật chất về vệ sinh thực tế hiện có của doanh nghiệp.
- Các thủ tục cần thực hiện: Mô tả chi tiết các thủ tục và thao tác phải thực hiện để đạt yêu cầu vệ sinh
- Phân công trách nhiệm thực hiện và quy định giám sát việc thực hiện SSOP.
b. Hình thức một Quy phạm vệ sinh chuẩn SSOP: được thể hiện dưới dạng văn bản, gồm hai phần:
- Các thông tin về hành chính (tên, địa chỉ công ty, tên sản phẩm hoặc nhóm sản phẩm, số và tên quy phạm, ngày và chữ ký phê duyệt của người có thẩm quyền),
- 4 nội dung chính nêu trên.
3.3. Các tài liệu khác:
- Văn bản quy định của pháp luật hiện hành.
- Các tiêu chuẩn, quy định kỹ thuật về thiết bị, nguyên liệu, sản phẩm, các yêu cầu thao tác kỹ thuật.
- Các bản vẽ thiết kế nhà xưởng, thiết bị.
- Các yêu cầu, phản hồi của khách hàng.
- Các thông tin khoa học mới
- Kinh nghiệm thực tiễn của doanh nghiệp
- Kết quả nghiên cứu/thử nghiệm mẫu …
II - TIÊU CHUẨN GLP-WHO:
- Hệ thống an toàn chất lượng phòng thí nghiệm GLP (Good Laboratory Practice - Thực hành tốt phòng thí nghiệm) là tất cả các hoạt động có hệ thống được hoạch định sẵn và áp dụng theo hệ thống chất lượng, thể hiện những yếu tố thích hợp nhằm đảm bảo độ tin cậy cần thiết đáp ứng được các yêu cầu chất lượng.
- Thực hành tốt phòng thí nghiệm (GLP) biểu hiện một tập hợp các nguyên tắc mà cung cấp một khuôn khổ trong đó các nghiên cứu trong phòng thí nghiệm được lên kế hoạch, thực hiện, theo dõi, ghi nhận, báo cáo và lưu trữ. Những nghiên cứu này được thực hiện để tạo dữ liệu mà các mối nguy hiểm và rủi ro cho người dùng, người tiêu dùng và các bên thứ ba, bao gồm cả môi trường, có thể được đánh giá cho dược phẩm (chỉ nghiên cứu preclinical), hóa chất nông nghiệp, mỹ phẩm, phụ gia thực phẩm, chất phụ gia thức ăn và các chất gây ô nhiễm, thực phẩm tiểu thuyết , biocides, chất tẩy rửa vv ... GLP giúp đảm bảo quyền quy định rằng các dữ liệu được gửi là một sự phản ánh thực sự của những kết quả đạt được trong thời gian nghiên cứu và do đó có thể được dựa theo khi đưa ra nguy cơ / đánh giá an toàn.
III - TIÊU CHUẨN GSP-WHO:
- Thực hành tốt bảo quản thuốc - Good Storage Practice (viết tắt : GSP) là các biện pháp đặc biệt, phù hợp cho việc bảo quản và vận chuyển nguyên liệu, sản phẩm ở tất cả các giai đoạn sản xuất, bảo quản, tồn trữ, vận chuyển và phân phối thuốc để đảm bảo cho thành phẩm thuốc có chất lượng đã định khi đến tay người tiêu dùng.
- GSP đưa ra các nguyên tắc cơ bản, các hướng dẫn chung về “Thực hành tốt bảo quản thuốc”, với 7 điều khoản và 115 yêu cầu. Tuy nhiên, các nguyên tắc, hướng dẫn này có thể được điều chỉnh để đáp ứng các yêu cầu cụ thể riêng biệt, nhưng vẫn đảm bảo thuốc có chất lượng đã định.
- GSP áp dụng cho các nhà sản xuất, xuất khẩu, nhập khẩu, buôn bán, tồn trữ thuốc.
IV - TIÊU CHUẨN CHO CÁC PHÒNG THÍ NGHIỆM AN TOÀN SINH HỌC:
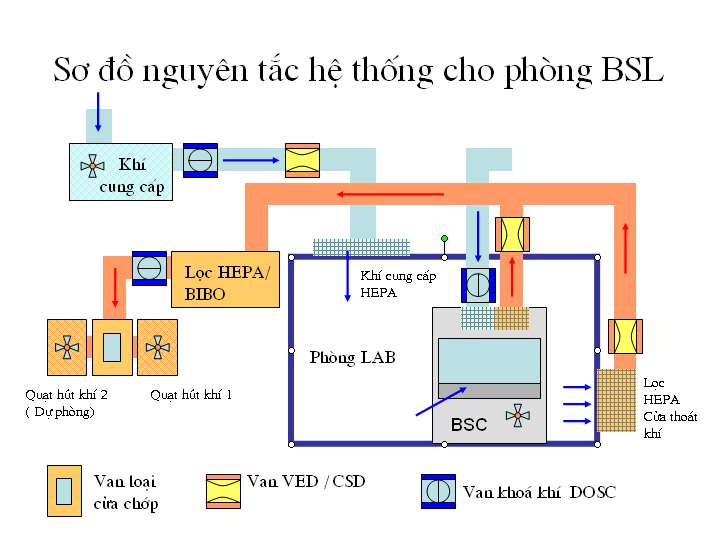
Sơ đồ nguyên tắc một hệ thống phòng An toàn sinh học (BSL)
1. Phân loại Phòng thí nghiệm An toàn sinh học (ATSH) theo các cấp độ:
- Phòng thí nghiệm An toàn sinh học cấp độ I (BSL-I): Là phòng thí nghiệm dùng để nghiên cứu và làm việc với các tác nhân sinh học nguy hiểm thuộc nhóm rủi ro số 1 (Risk Group 1 - RG 1), là các chất không gây phát bệnh đối với người lớn khoẻ mạnh.
- Phòng thí nghiệm An toàn sinh học cấp độ II (BSL-II): Là phòng thí nghiệm dùng để nghiên cứu và làm việc với các tác nhân sinh học nguy hiểm thuộc nhóm rủi ro số 2 (Risk Group 2 - RG 2), là các chất có thể gây nhiễm bệnh cho người nhưng không nguy hiểm, có phương pháp cứu chữa và điều trị.
- Phòng thí nghiệm An toàn sinh học cấp độ III (BSL-III): Là phòng thí nghiệm dùng để nghiên cứu và làm việc với các tác nhân sinh học nguy hiểm thuộc nhóm rủi ro số 3 (Risk Group 3 - RG 3), là các chất gây ra bệnh nguy hiểm hoặc bệnh chết người, có phương pháp điều trị.
- Phòng An toàn sinh học cấp độ IV (BSL-IV): Là phòng thí nghiệm dùng để nghiên cứu và làm việc với các tác nhân sinh học nguy hiểm thuộc nhóm rủi ro số 4 (Risk Group 4 - RG 4), là các chất gây ra bệnh nguy hiểm chết người, không có phương pháp điều trị và cứu chữa, hoặc các chất nguy hiểm chưa được biết đến.
2. Các tiêu chí của cấp độ ATSH phòng thí nghiệm:
- ATSH cấp độ 1 (BSL-1): phù hợp với công việc liên quan đến các tác nhân đặc trưng chưa được xác định là không gây bệnh cho những người lớn tuổi khỏe mạnh và chỉ có những nguy cơ rất nhỏ đối với các nhân viên phòng thí nghiệm và môi trường xung quanh. Một phòng thí nghiệm không nhất thiết phải phân chia thành nhiều khu trong một tòa nhà. Công việc chủ yếu được thực hiện trên mặt các bàn thí nghiệm mở theo các phương pháp thực hành vi sinh tiêu chuẩn. Các trang thiết bị phòng tránh đặc biệt hoặc thiết kế cơ sở vật chất không được yêu cầu cung cấp cũng như sử dụng. Nhân viên phòng thí nghiệm được đào tạo cụ thể về các quy trình liên quan đến phòng thí nghiệm và được giám sát bởi một nhà khoa học đã có kiến thức về vi sinh hoặc khoa học tương tự.
- ATSH cấp độ 2 (BSL-2): tương tự như ATSH cấp độ 1 và phù hợp cho công việc liên quan đến các tác nhân có mức độ nguy hiểm đối với nhân viên và môi trường ở mức trung bình. Những điểm khác biệt của BSL-2 so với BSL-1 ở chỗ: (1) nhân viên phòng thí nghiệm phải được đào tạo chi tiết về phương pháp xử lý các tác nhân gây bệnh và làm việc dưới sự hướng dẫn của các nhà khoa học xuất sắc; (2) khu vực tiếp cận phòng thí nghiệm được kiểm soát khi công việc đang được tiến hành; (3) các biện pháp phòng tránh được thực hiện với các vật sắc nhọn nhiễm bệnh; (4) các quy trình tạo ra các soi khí nhiễm bệnh hoặc có sự bắn tóe dung dịch thì được thực hiện trong các tủ ATSH hoặc các thiết bị phòng tránh cho cơ thể khác.
- ATSH Cấp độ 3 (BSL-3): được áp dụng cho các phòng thí nghiệm lâm sàng, chẩn đoán, đào tạo, nghiên cứu và sản xuất và các công việc được thực hiện với các tác nhân trong nước hoặc tác nhân nước ngoài có thể gây ra những căn bệnh nguy hiểm hoặc có nguy cơ tử vong cao thông qua con đường hô hấp. Nhân viên phòng thí nghiệm phải trải qua khóa đào tạo về xử lý các tác nhân gây bệnh hoặc có nguy cơ gây chết người và phải được giám sát bởi các nhà khoa học xuất sắc có nhiều kinh nghiệm làm việc với các tác nhân này.
Toàn bộ quy trình liên quan đến việc thao tác với các mẫu vật nhiễm bệnh đều được thực hiện bên trong các tủ ATSH hoặc các thiết bị phòng tránh vật lý khác hoặc các nhân viên phòng thí nghiệm phải mặc quần áo và đeo các dụng cụ bảo hộ cá nhân phù hợp.
Phải công nhận rằng những phòng thí nghiệm đã xây dựng trước đó không thể có đầy đủ những tiêu chuẩn đáp ứng ATSH Cấp độ 3 (Ví dụ: Khu vực ra vào có cửa đôi và kín khí). Trong trường hợp này, cấp độ ATSH phù hợp để thực hiện các quy trình như bình thường (ví dụ: các quy tình chẩn đoán liên quan đến sự lan truyền của tác nhân để xác định, phân loại, kiểm tra tính mẫn cảm, v.v...) là ATSH Cấp độ 2, bao gồm: 1) Khí thải từ phòng thí nghiệm được thải ra bên ngoài trời; 2) hệ thống thông gió cho phòng thí nghiệm được lắp đặt để cấp khí vào trong các phòng; 3) cửa ra vào phòng thí nghiệm bị hạn chế khi công việc đang được thực hiên; 4) Các phương pháp thực hành Vi sinh tiêu chuẩn, Các phương pháp thực hành đặc biệt và Trang thiết bị bảo hộ thuộc ATSH Cấp độ 3 phải được thực hiện nghiêm ngặt. Giám đốc phòng thí nghiệm là người duy nhất đưa ra quyết định thực hiện việc điều chỉnh các tiêu chuẩn của ATSH Cấp độ 3.
- ATSH Cấp độ 4 (BSL-4): được quy định cho các công việc thực hiện với các tác nhân nguy hiểm và tác nhân nước ngoài, những tác nhân gây ra những nguy cơ bị nhiễm các bệnh truyền nhiễm của phòng thí nghiệm thông qua con đường sol khí và các bệnh đe dọa đến tính mạng cho từng cá nhân riêng lẻ. Các tác nhân có mối quan hệ sinh kháng thể gần gũi hoặc giống với các tác nhân thuộc ATSH cấp độ 4 cũng được áp dụng theo cấp độ 4 này cho đến khi nhận được các dữ liệu đầy đủ để khẳng định có thể tiếp tục công việc với các tác nhân theo cấp độ 4 hay là áp dụng một cấp độ thấp hơn. Các nhân viên của phòng thí nghiệm phải trải qua khóa đào tạo về thao tác với các tác nhân gây bệnh cực kỳ nguy hiểm và họ phải nắm bắt được các chức năng phòng ngừa sơ cấp và thứ cấp của các phương pháp thực hành đặc biệt và tiêu chuẩn, trang thiết bị bảo vệ và các đặc điểm thiết kế phòng thí nghiệm. Các nhân viên thường được giám sát bởi các nhà khoa học dày dặn kinh nghiệm và đã qua đào tạo về thực hành với các tác nhân kể trên. Giám đốc phòng thí nghiệm phải kiểm soát nghiêm ngặt khu vực tiếp cận của phòng thí nghiệm. Khu phòng thí nghiệm phải là một tòa nhà tách biệt hoặc nằm trong một khu vực được kiểm của tòa nhà và được cách ly với các khu vực khác. Cần có một cuốn cẩm nang vận hành phòng thí nghiệm.
Tại các khu vực làm việc của phòng thí nghiệm, toàn bộ hoạt động đều được thực hiện trong các tủ ATSH Cấp độ III hoặc sử dụng tủ ATSH cấp độ II nhưng nhân viên phải mặc quần áo bảo hộ một mảnh có áp suất dương được thông hơi bằng một hệ thống hỗ trợ có độ bền cao. Phòng thí nghiệm ATSH cấp độ 4 phải có những đặc điểm thiết kế và xây dựng chống sự phân tán của các vi sinh vật từ phòng thí nghiệm ra môi trường bên ngoài.
(Dựa theo các nguồn của WHO)